Je besser die IT-Lösung,
desto erfolgreicher die Studie.
CentraXX Trial – Die Planung und Durchführung von Studien sind elementare Bestandteile der klinischen Forschung. Doch oft sieht man sich schon in der Projektierungsphase mit immensen Problemen konfrontiert. Allein die Rekrutierung der kritischen Teilnehmerzahl von Patienten mit den für die Studie relevanten Kriterien stellt sich häufig als kompliziert und langwierig heraus. Abhilfe schafft hier CentraXX Trial – das Studienmodul der CentraXX-Produktfamilie.
Hauptaufgabe und Bestandteil des Studienmanagementmoduls CentraXX Trial ist die strukturierte Datenerfassung und -haltung, die die Grundlage der Studiendaten-Speicherung, des Reportings und der Analyse darstellen. Auch hierbei bietet die integrierte Workflow Engine eine systematische Ablaufunterstützung für die qualitätsgesicherte Studiendurchführung. Damit ist CentraXX Trial in der Lage, alle relevanten Vereinbarungen aus dem Studienablaufplan und dem Studiendesign populationsbasierter, versorgungsnaher oder klinischer Studien abbilden zu können.
Studienregister
Voraussetzung für eine campusweite Rekrutierung ist die Registrierung und übersichtliche Darstellung aller Studien in einem Portal. Im Studienregister, lassen sich diverse Studienprofile, bestehend aus unterschiedlichsten Dokumentationspunkten mit verschiedenen Ausprägungen und Vokabeln, abbilden. Zum einen erlaubt dies die Sortierung nach individuellen Forschungsfeldern und den großen Volkskrankheiten. Zum anderen werden Ein- und Ausschlusskriterien aller Studien strukturiert erfasst.
Somit kann der gesamte Patienten-/Probandenbestand mit all ihren strukturierten Daten (Therapie, Diagnosen, Proben etc.) in CentraXX gezielt nach potentiellen Studienteilnehmern durchsucht werden. Dieser Mechanismus verbessert einerseits die Durchführung von Machbarkeitsstudien. Hierdurch wird die Wahrscheinlichkeit von Low-Performern minimiert, mit dem Ergebnis von Kostensenkungen.
Nach einer erfolgreich abgeschlossener Machbarkeitsstudie liefert CentraXX innerhalb der Einschleusungsphase unter Berücksichtigung aller hinterlegten Ein- und Ausschlusskriterien automatisierte Rekrutierungsvorschläge (z.B. aus Tumorkonferenzen).
Studienverlaufsdokumentation
Bereits bei der Erstellung des Studiendesigns unterstützt CentraXX den PI aktiv.
Nach erfolgter Rekrutierung des Patienten/Probanden
Fazit:
KAIROS schlägt mit CentraXX den Bogen vom Biobanking zum Studienmanagement und hilft, die relevanten Daten aus beiden Bereichen sinnvoll und nutzbringend zu verbinden.
Aufklärung, Einwilligung sowie Planungen von Therapien und Operationen sind weitere wesentliche Schritte. Es folgt die Entnahme von Bioproben, ihre Lagerung und Analyse sowie die Dokumentation aller Schritte. Studien Reporting wird da schnell zur Sisyphusarbeit. KAIROS schlägt den Bogen vom Biobanking zum Studienmanagement und hilft Ihnen, die relevanten Daten aus beiden Bereichen sinnvoll und nutzbringend zu verbinden.
Auch das Rekrutieren von Patienten (Einschleusung) und das vorzeitige Beenden (Erreichung von Abbruchbedingungen) werden von CentraXX Trial abgebildet. Mithilfe dieser Systemwerkzeuge unterstützt CentraXX die Durchführung multizentrischer Studien, integrierte Abläufe und gewährt jederzeit größtmögliche Transparenz.
Zentrale Speichereinheit von Daten ist die patientenzentrierte Studienakte, die Studienprotokolle in Form von digitaler Abbildungen strukturiert und dem Probanden eindeutig zuordnet.
Die CentraXX-Studienakte ist der verlängerte Arm der KIS EPA hinein in die Forschung. Die Anpassung an neue Studien erfolgt über die Verwendung vorgefertigter und veränderbarer eCRFs. Diese elektronischen Case Report Forms sind die Grundlage der Studiendokumentation, die per Verarbeitungsschicht angeboten werden. Studienabläufe können vorab als sog. Swim-Lane-Modelle definiert und visualisiert werden. Die Überwachung, Orchestrierung und Protokollierung erfolgt durch die integrierte Workflow Engine. Durch Aufgabenlisten, Status-Flags und die Leistungserfassung ist es jederzeit möglich, den Bearbeitungsstatus zu einem bestimmten Patienten zu prüfen. Die Informationen zu den entnommenen Bioproben, die Patienteneinwilligungen und andere Informationen komplettieren die Studienakte als zentrales Probanden-Informations- und -Austauschmedium.
Neben der jeweiligen Studienakte als Informations- und Funktionscontainer verfügt CentraXX Trial über ein integriertes Diskussionsforum. Über diesen „Kanal“ können rollenübergreifend Aufgaben organisiert werden und unmittelbar patientenbezogen Ideen ausgetauscht werden. Das Studienforum bietet Aktivitätslisten zum Verweis in die Studien-Workflows, Blog-Funktionen zu Kommunikationszwecken und synchronisierte Statusinformationen aus der aktuellen Studie.
Mit Blick auf die hohen Anforderungen an die Dokumentationsqualität beim Studienmanagement ist das Studienforum ein wertvolles Werkzeug. Schließlich sind neue Entdeckungen, aus denen möglicherweise neue Schlussfolgerungen abgeleitet werden, zu belegen und für die gesamte Studienentwicklung aufzuzeigen.
Außerdem sind in der Forschung nicht nur die Entscheidung für eine Therapie und das Ergebnis wichtig, sondern auch die vorausgehende Intention, d.h. die Überlegungen zur Diagnose und die Gründe, die zur Wahl der Therapie geführt haben. Das integrierte Studienforum geht über den Blick in die Befundbriefe hinaus und bietet optimale Möglichkeiten, sich in Überlegungen anderer hineinzudenken. Letztlich wurden die klassischen Funktionen eines Webforums umgesetzt. Dies hat den Vorteil, dass man direkt in Bezug zu einer Studie, einem Patienten oder einer Untersuchung Diskussionsbeiträge schreiben kann. Dies ist für das Zusammenwirken des forschenden Personals von großer Wichtigkeit. Die Beiträge können mit Schlagworten, Blogs, Themen oder auch mit Bildern, Filmen, Links ergänzt werden. Publikationshilfen und Werkzeuge zur selbständigen Modellierung runden das CentraXX-Studienmanagement, das sich in sieben Phasen gliedern lässt, ab.
CentraXX Trial im Überblick:
Schon zum Zeitpunkt der initialen Studiendefinition kann Ihnen CentraXX helfen. So ist es ein Leichtes, über Abfragen, Suchen und Analysen die Machbarkeit einer Studie zu bestimmen. Sie können feststellen, wie das Probandenaufkommen in der Vergangenheit bei vergleichbaren Studien war, oder wie die Rekrutierung in der Vergangenheit ausgefallen wäre. Damit können Sie schon mit der Studiendefinition “low performer” ausschließen.
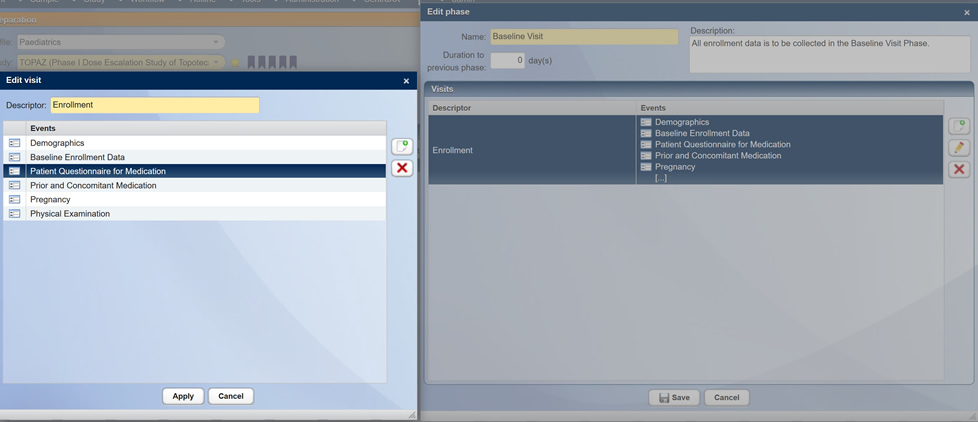
Studienlayout/-Designtools in CentraXX
Sobald Studien durch die Ethikkommission oder auch durch Ihren Sponsor freigegeben wurden, können Sie die dazugehörigen Dokumente der Studie hinzufügen und haben diese für Sie und die ausgewählten Projektmitarbeiter jederzeit und überall im Zugriff. Schon zu diesem Zeitpunkt haben Sie die Möglichkeit, die Einwilligungserklärungen strukturiert im System zu hinterlegen.
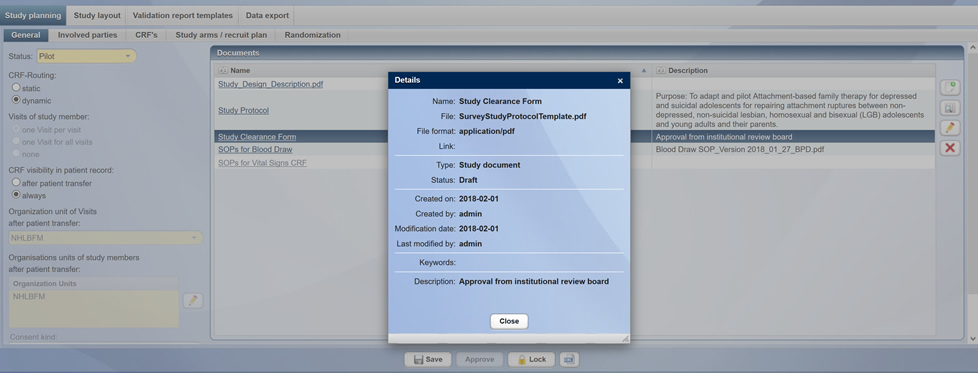
Speichern und Darstellung der Studienfreigabedokumente (Ethikkommission/Sponsor)
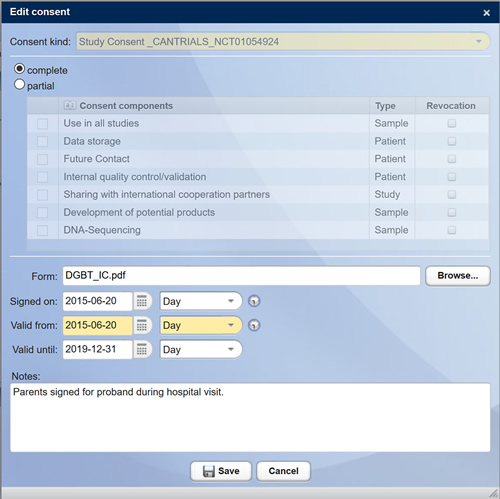
Strukturierte Erfassung und Darstellung der Einwilligungserklärungen
Über ein eigenes webbasiertes Administrationstool können Sie selbst ohne langes Warten und ohne Softwarekenntnisse die Studienteilnehmer und Ressourcen für Ihre Studie festlegen. Die so definierte Studie wird im CentraXX-Studienregister publiziert, so dass allen Berechtigten der Zugang zu wichtigen Studieninformationen wie Ein- und Ausschlusskriterien sofort möglich ist.
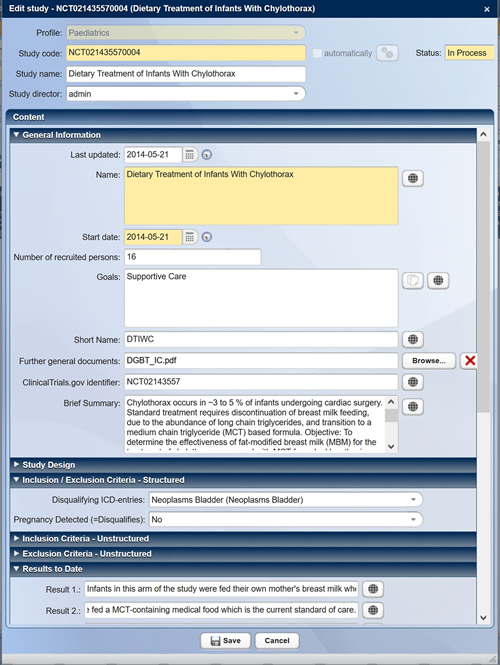
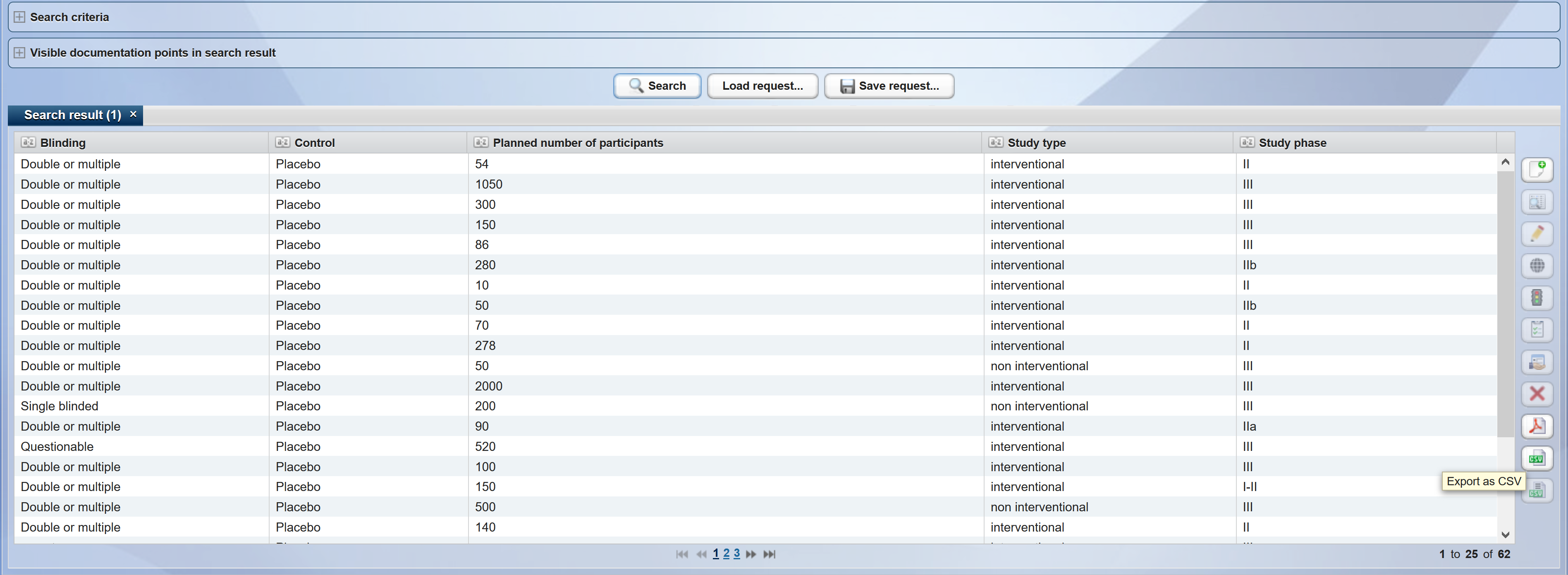
Strukturierte Erfassung und Darstellung der Studien im Studienregister
In CentraXX Trial steht Ihnen ein Rekrutierungsagent zur Verfügung. So wird der anonymisierte Aufnahmedatensatz durchsucht oder es werden, beispielsweise in der Onkologie, die Patienten zum Zeitpunkt der Tumorkonferenz vom System als Studienteilnehmer bei entsprechender Übereinstimmung mit den Ein- und Ausschlusskriterien anonymisiert angezeigt. So können Sie den behandelnden Arzt auf eine Studie aufmerksam machen und um Rekrutierungsunterstützung bitten.
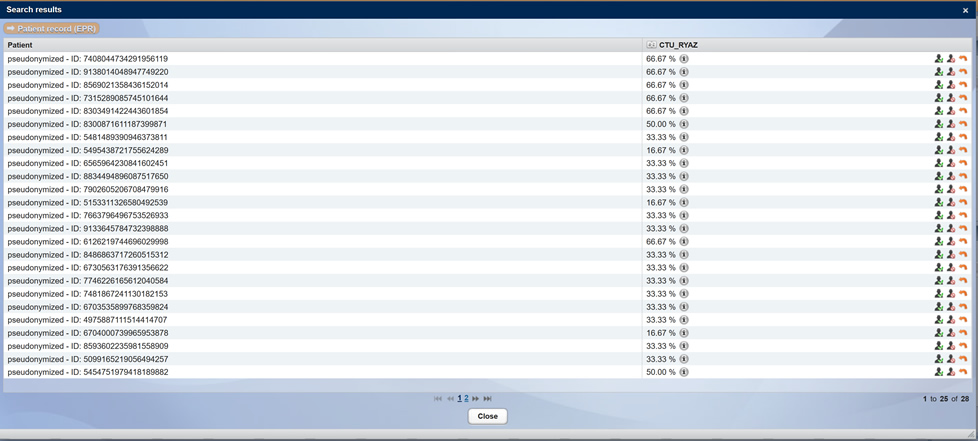
Anonymisierte Darstellung geeigneter Studienteilnehmer
Zentrales Element ist der eCRF Designer. Er ermöglicht die flexible Gestaltung von Formularen, die für eine Studiendokumentation benötigt werden. Daher geht es bei den elektronischen Case Report Forms (eCRF) um eine Unterstützung entlang des gesamten Lebenszyklus der eCRFs, also vom Design über Test und Nutzung bis hin zur Archivierung und einem begleitenden Änderungsmanagement (Versionierung). Das eCRF-Modul entspricht funktional dem Modul Formularmanagement beim klinischen KAS. Die skizzierte Gestaltung findet sich auch in der Grundüberlegung von CentraXX zur Umsetzung dieses bedeutenden Tools wieder. Über die Rolle des e-CRF-Designers und seine Einbettung im Bereich Workflow/Rules Engine und Data Dictionary bietet das Studienmanagement weitere wesentliche Funktionen an, um z.B. AMG-Studien vollumfänglich abzubilden:
- Discrepancy Management und Reporting
- CRF-Monitoring
- job-gesteuerte Überprüfung
- Dokumentation von adverse Events.
Neben der Dokumentation und dem Monitoring der Studie ist es wichtig, jederzeit auch Managementinformationen zu erhalten. Wenn Sie über alle Studien Ihrer Einrichtung wichtige Kennzahlen abfragen und analysieren wollen, hilft Ihnen das Reporting Werkzeug von CentraXX.
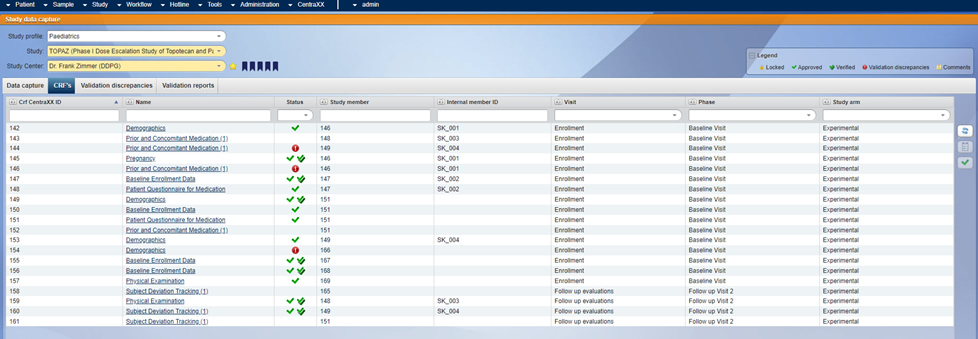
Darstellung eines Validierungsverstoßes im selbstdesignten eCRF
Die Darstellung von Studienergebnissen wird nicht nur in Grafiken und Tabellen im System vorgenommen, sondern Sie können auch Studien mit vergleichbaren Ergebnissen zur Analyse heranziehen. So können Sie das für weiterführende Untersuchung wichtige Benchmarking im System CentraXX vornehmen.
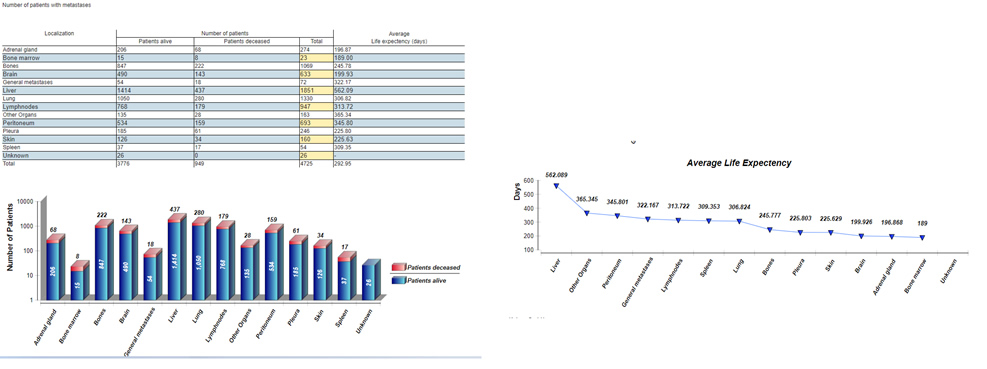
Darstellung von Studienergebnissen in Grafiken und Tabellen
Schließlich wollen Sie eine sehr einfache Publikation Ihrer Ergebnisse.
Ähnlich der Befundbriefbeschreibung aus dem Klinikalttag funktioniert die CentraXX Publikationshilfe. Dieses Werkzeug ermöglicht die Auswahl aller wichtigen Ergebnisse und den Export an ein Textverarbeitungs- oder Tabellenkalkulationsprogramm.
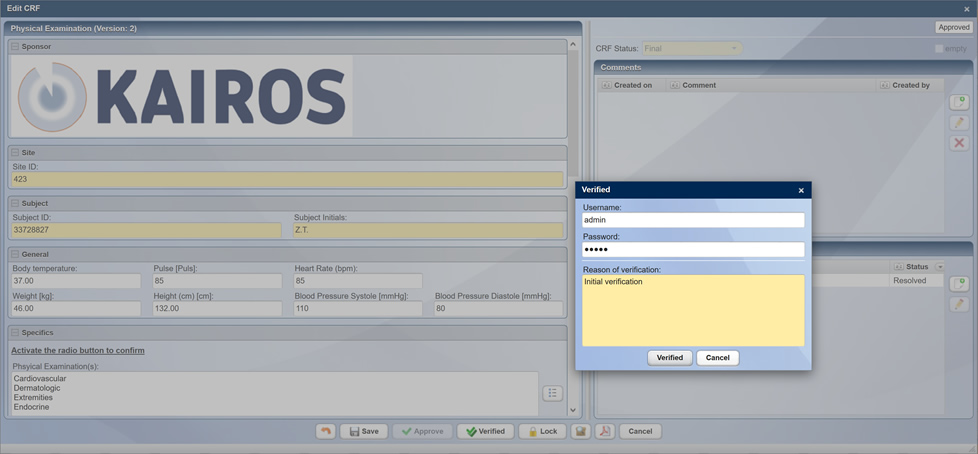
Detailinformationen zu CentraXX Trial finden Sie auf dem Produktblatt.
Für Ihre Fragen rund um dieses Angebot steht Ihnen als direkter Ansprechpartner Stephan Reschke zur Verfügung:
Selbstverständlich können Sie sich auch – z.B. zur Vereinbarung eines Präsentationstermins – telefonisch unter 0234 58882110 oder per E-Mail an wenden. Denn: die Zeit ist jetzt.



